domingo, 22 de mayo de 2011
sábado, 19 de marzo de 2011
4º - Guía de Nomenclatura 1
Les solicito la impriman ya que trabajaremos con ella en clase.
Será complementada con diversos esquemas que irán apareciendo en el blog.
lunes, 24 de mayo de 2010
4º - Obtención de óxidos ácidos: algunos aspectos
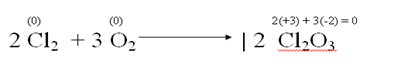
1. El cloro y el oxígeno tienen atomicidad 2 porque sus respectivas moléculas están formadas por dos átomos de cloro y de oxígeno.
2. Las sustancias simples tiene número de oxidación = 0
3. El cloro se oxida porque su número de oxidación aumenta de 0 a +3.
4. El oxígeno se reduce porque su número de oxidación disminuye de 0 a -2.
5. Por estas razones, las reacciones de obtención de óxidos son oxidorreducciones o reacciones rédox.
5º -Guía de nomenclatura de alcanos
Llévenla al colegio para aplicarla retroactivamente a los compuestos que formulamos en clase.
sábado, 15 de mayo de 2010
4º - Números de Oxidación 1
viernes, 14 de mayo de 2010
4º - Fórmulas generales de la funciones químicas
Función química | Fórmula general | Ejemplo |
OXIDO BASICO | MaOb | Fe2O3 |
OXIDO ACIDO | NaOb | Cl2O3 |
OXACIDO | HaNbOc | HClO2 |
HIDROXIDO | M(OH)n | Fe(OH)3 |
HIDRURO METALICO | MHn | FeH3 |
HIDRURO NO METALICO o HIDRACIDO | HnN | HCl |
El cloro, con Nox = +3 en el óxido ácido y en el oxácido y con
Nox = -1 en el hidrácido.
domingo, 16 de agosto de 2009
4º - Actividad para el receso invernal resuelta
La idea es que además de leerla, la impriman y confronten con lo que escribieron ustedes en los primeros minutos de la clase del próximo miércoles, antes de la evaluación.(si logro corregirlos...)
Lean las guías de nomenclatura, lo escrito en clase y todo el material que figura aquí en el blog.
Como se darán cuenta, sales binarias y oxosales, son temas que implican conocimiento de los compuestos vistos anteriormente, particularmente oxácidos, hidrácidos e hidróxidos.
miércoles, 27 de mayo de 2009
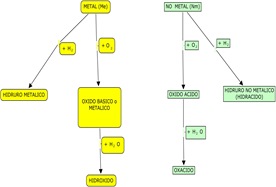
4º - Árbol de Obtenciones
Aparecen aquí vinculadas las diferentes reacciones de obtención que aprendimos durante el trimestre.
lunes, 2 de junio de 2008
4º - Consultas de Agostina y Mauro
Agostina Salman y Mauro Maiana, han realizado una serie de consultas muy específicas que me parece oportuno postear aquí:
¿a qué se refiere con Principio de conservación de la masa?
En una ecuación química, la cantidad de átomos de cada elemento a ambos lados de la flecha es la misma. (en el 2º trimestre, en estequiometría, ampliaremos este concepto)
Haciendo resúmenes nos surgieron algunas preguntas, ojalá pueda contestárnoslas.
1) Si un elemento tiene tres Nox, ¿a cuál se le coloca el sufijo -oso o -ico? ¿a alguno se le coloca el prefijo hipo- o per-?
La respuesta está en la guía de nomenclatura.(vean también el caso del manganeso)
2) ¿Cómo sería la nomenclatura con numeral de stock y la estequiometrica del hidruro de arsénico (Nox: -3)?.
Para los hidruros no metálicos hay dos nombres tradicionales (arseniuro de hidrógeno y ácido arsenhídrico) y no se utiliza la nomenclatura con numeral de Stock. En cuanto a la sistemática, podemos llamarlo trihidruro de arsénico.
3) Al hidrógeno se lo considera protón en una disociación de un metal con agua, ¿es lo mismo que catión?
El protón surge en la disociación del agua, de un oxácido o de un hidrácido. No hay "disociación de un metal con agua". El protón es un catión, ya que es un ion con carga positiva.
La disociación del agua también produce un oxhidrilos, que formarán parte de los hidróxidos.(ver obtención de hidróxidos y mecanismo de disociación del agua en la carpeta).
4) ¿Cómo sé cuál Nox usar en una ecuación de obtención de oxácidos cuando el no metal tiene más de un Nox?
A partir del nombre del oxácido que se quiere obtener o de su fórmula molecular se deduce el Nox del no metal que lo integra (Ese número será uno de los que figure en la tabla periódica, además)
En el óxido ácido a partir del cual se obtiene el oxácido, el número de oxidación del no metal es el mismo que en el oxácido.
Si no comprendieron alguna parte trataré de ampliar.
martes, 23 de octubre de 2007
3º - Números de oxidación (62)
Recuerden que:
1. Sustancia simple es aquélla cuyas moléculas están formadas por átomos de un elemento.
2. Sustancia compuesta binaria o compuesto binario es la sustancia cuyas moléculas están formadas por átomos de dos elementos.
Lleven este cuadro a la clase del jueves 25-10